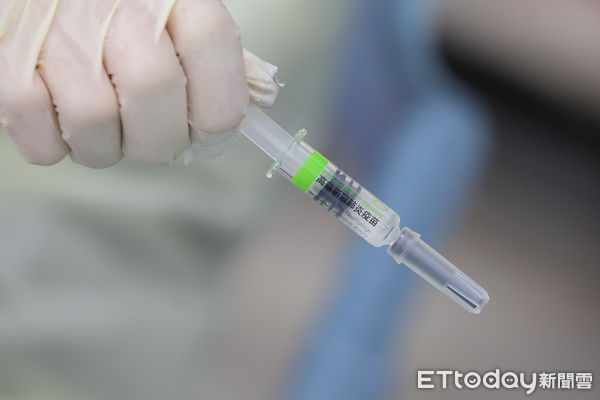
▲日本不接受高端疫苗。(圖/記者湯興漢攝)
記者吳珍儀/台北報導
日本開放邊境卻不接受高端疫苗,各界批評聲浪四起,高端疫苗公司今日發出聲明,強調3大重點,聲明中也強調,由於日本不接受高端疫苗原因在於台灣並非WHO成員國,高端疫苗無法於取得台灣認證後直接申請WHO認證,需經第3國藥監單位的協助,已向澳洲政府提出申請。
高端疫苗公司網站上發出聲明,強調3大回應:
1. 關於日本入境檢疫規定,日本目前入境檢疫規定僅接受WHO緊急使用清單(EUL) 的新冠疫苗接種證明,不包含已取得台灣EUA的高端疫苗。
高端新冠疫苗依循台灣法規單位之標準進行開發,為台灣認可之正式EUA疫苗;日本入境檢疫要求並非藥證申請審查,不屬於廠商主動向日本政府藥監單位提出申請之事項。因此,高端疫苗已於9月份提供疫情指揮中心相關文件,並陸續提供其他補充資料,協助政府部門進行溝通。高端疫苗將配合台日雙方政府持續協商,盼盡快提供民眾更便利的赴日旅遊方式。
2. 國際認證進度方面,高端新冠疫苗因良好的研發成果受到WHO肯定,進而入選團結試驗疫苗(STV),由WHO主導執行全球臨床三期,目前靜待其公佈臨床結果;此外,高端疫苗也自行於國外執行免疫橋接三期試驗。
台灣非WHO成員國,高端疫苗無法於取得台灣認證後直接申請WHO認證,需經第三國藥監單位的協助,才得以提出申請。目前高端疫苗已向澳洲藥監單位TGA及WHO相關主管部門正式提出申請緊急使用許可,如有任何進度更新,即依法規公告。
台灣因政治處境特殊,台灣本土疫苗廠欲取得國際認證之難度遠高於其他國外疫苗公司。雖有此客觀限制條件,高端疫苗全體員工仍將全力以赴,為國際認證之目標努力。
3.關於疫苗保護效益(effectiveness)報告,高端新冠疫苗於2021年取得台灣緊急使用授權 (EUA) 時,衛福部食藥署要求於今年(2022)檢送疫苗保護效益(effectiveness)報告,本公司已如期繳交,並於專家會議上報告說明。日前收到食藥署審查補件要求後,已積極準備相關資料,將依要求及規範如期於10月底完成補件。





讀者迴響